Aldehyder: struktur, egenskaper, nomenklatur og anvendelser eksempler
Aldehydene er organiske forbindelser som har den generelle formel RCHO. R representerer en alifatisk eller aromatisk; C til karbon; Eller oksygen og H til hydrogen. De er kjennetegnet ved en karbonylgruppe som ketoner og karboksylsyrer, så aldehyder er også referert til som karbonylforbindelser.
Karbonylgruppen gir aldehydet mange av dets egenskaper. De er forbindelser som lett oksyderer og er svært reaktive mot nukleofile tilsetninger. Dobbeltbindingen av karbonylgruppen (C = O) har to atomer, som har forskjeller i aviditet for elektroner (elektro).
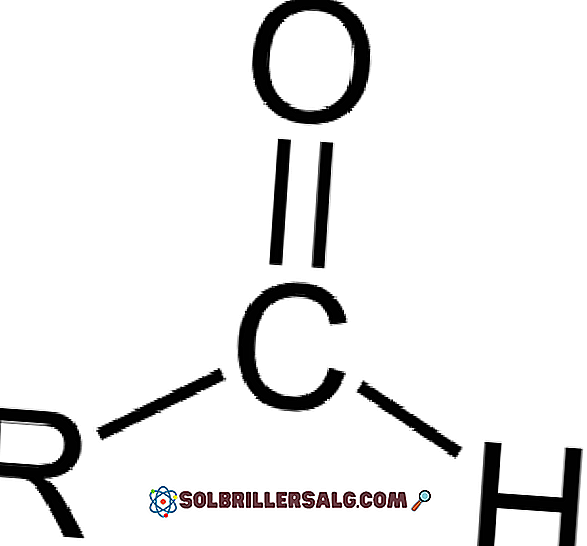
Oksygen tiltrekker seg elektroner sterkere enn karbon, så den elektroniske skyen beveger seg mot den som gjør dobbeltbindingen mellom karbon og oksygenpolar, med et viktig dipolmoment. Dette gjør aldehyder polare forbindelser.
Polaritet av aldehyder vil påvirke de fysikalske egenskaper. Kokpunktet og oppløseligheten av aldehyder i vann er større enn ikke-polare kjemiske forbindelser med lignende molekylvekter, slik er det tilfelle av hydrokarboner.
Aldehyder med mindre enn fem karbonatomer, er oppløselig i vann, ettersom hydrogenbindinger mellom oksygenet av karbonylgruppen og vannmolekylet dannes. Økningen av karbonnummeret i hydrokarbonkjeden resulterer imidlertid i en økning i den ikke-polare delen av aldehydet, noe som gjør den mindre løselig i vann.
Men hvor de er og hvor de kommer fra? Selv om i det vesentlige avhengig av arten av karbonylgruppen, resten av molekylstrukturen bidrar også mye for å angi. Dermed kan de være av hvilken som helst størrelse, liten eller stor, eller til og med en makromolekyl kan ha regioner der karakteren av aldehyder dominerer.
Således, som med alle kjemiske forbindelser, er det "hyggelige" aldehyder og andre bittere. De kan finnes i naturlige kilder eller syntetisert i stor skala. Eksempler på aldehyder er vanillin, veldig tilstede i iskrem (toppbilde) og acetaldehyd, som tilsetter smaken til alkoholholdige drikkevarer.
Kjemisk struktur

Aldehyder består av en karbonyl (C = O) som et hydrogenatom er direkte koblet til. Dette skiller seg fra andre organiske forbindelser, slik som ketoner (R 2 C = O) og karboksylsyrer (R-COOH).
I den ovennevnte bilde molekylstrukturen rundt -CHO formylgruppen vist. Formylgruppen er flatt, fordi karbon og oksygen er sp2 hybridisert. Denne planariteten gjør den mottakelig for angrepet av nukleofile arter, og oksyderer derfor lett.
Hva refererer denne oksidasjonen til? Til dannelsen av en binding med noe annet atom mer electronegative enn karbon; og i tilfelle av aldehyder er det et oksygen. Således omsettes aldehydet oksyderes til en karboksylsyre, -COOH. Hva om aldehydet ble redusert? En primær alkohol, ROH, ville bli dannet i sin plass.
Aldehyder fremstilles kun fra primære alkoholer: de hvor OH-gruppen ved enden av en kjede. På lignende måte er formylgruppen alltid på enden av en kjede eller stikker ut fra den eller ringen som en substituent (hvis det er andre viktige grupper, så som -COOH).
Fysiske og kjemiske egenskaper
Som polære forbindelser er deres smeltepunkter høyere enn de for ikke-polare forbindelser. Aldehyd-molekyler ikke er i stand til å binde intermolekylært med hydrogen, ved å ha bare karbonatomer bundet til hydrogenatomer.
På grunn av ovenstående har aldehyder lavere kokepunkter enn alkoholer og karboksylsyrer.
Smeltepunkt
Formaldehyd -92; Acetaldehyd -121; -81 propionaldehyd; n-butyraldehyd -99; n-Valeraldehyd-91; Caproaldehyd -; Heptaldehyd - 42; Fenylacetaldehyd -; Benzaldehyd -26.
Kokepunkt
Formaldehyd -21; Acetaldehyd 20; Propionaldehyd 49; n-butyraldehyd 76; n-Valeraldehyd 103; Caproaldehyd 131; Heptaldehyd 155; Fenylacetaldehyd 194; Benzaldehyd 178
Løselighet i vann uttrykt i g / 100 g H20
Formaldehyd, meget løselig; Acetaldehyd, uendelig; Propionaldehyd, 16; n-butyraldehyd, 7; n-valeraldehyd, svakt løselig; caproaldehyd, lite løselig; Litt løselig fenylacetaldehyd; Benzaldehyd, 0, 3.
Kokepunktene for aldehyder har en tendens til å øke direkte med molekylvekten. Tvert imot er det en tendens til å redusere aldehydernes løselighet i vann når deres molekylvekt øker. Dette gjenspeiles i de fysiske konstanter av de nevnte aldehyder.
reaktivitet
Oksidasjonsreaksjon
Aldehyderne kan oksyderes til den tilsvarende karboksylsyre i nærvær av noen av disse forbindelser: Ag (NH3) 2, KMnO4 eller K2Cr2O7.
Reduksjon til alkoholer
De kan hydrogeneres ved hjelp av nikkel-, platin- eller palladiumkatalysatorer. Således transformeres C = O til C-OH.
Reduksjon til hydrokarboner
I den nærvær av Zn (Hg), konsentrert HCl eller NH2 NH 2 aldehyder miste karbonylgruppen og blir hydrokarboner.
Nukleofil Tilsetning
Det er flere forbindelser som tilsettes til karbonylgruppen, blant dem er: Grignard-reagenser, cyanid, ammoniakkderivater og alkoholer.
nomenklatur
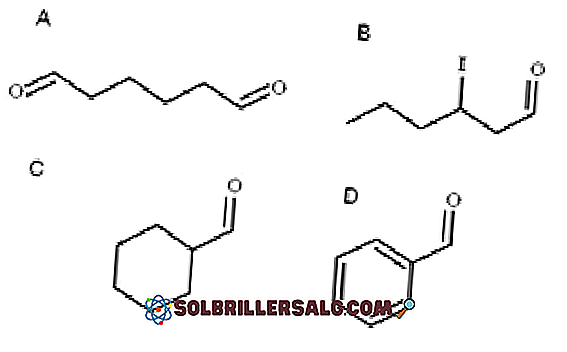
I de ovennevnte bilde fire aldehyder er illustrert. Hvordan heter de?
Gitt at de oksideres primære alkoholer, blir alkoholens navn endret til -ol ved -al. Således blir metanol (CH30H) hvis oksidert til CH3CHO kalt metanal (formaldehyd); CH3 CH2 CHO etanal (acetaldehyd); CH3CH2CH2CHO propanal og CH3CH2CH2CH2CHO butanal.
Alle de nylig nevnte aldehyder har -CHO-gruppen i enden av kjeden. Når det er i begge ender, som i A, i slutten -al legges prefikset di-. Som A har seks karboner (telle både formyls grupper) avledet fra 1-heksanol og navnet er det derfor: heksan hjulet.
Når det er en substituent, så som et alkylradikal, en dobbelt- eller trippelbinding eller et halogen, er kjolene i hovedkjeden oppført som gir -CHO-tallet 1. Således kalles aldehyd B: 3-jodhexanal.
I aldehyder C og D har imidlertid -CHO-gruppen ikke prioritet for å identifisere nevnte forbindelser fra andre. C er et cykloalkan, mens en benzen D, begge med en av de H-substituert med en formylgruppe.
I dem, som hovedstrukturen er syklisk, kalles formylgruppen karbaldehyd. Således er C cykloheksankarbaldehyd, og D den bencenocarbaldehído (kjent som benzaldehyd).
søknader
Det finnes aldehyder i naturen som er i stand til å gi behagelige smaker, slik er det tilfelle av cinnamaldehyd, som er ansvarlig for den karakteristiske smaken av kanel. Det er derfor de ofte brukes som kunstig smak i mange produkter som søtsaker eller mat.
formaldehyd
Formaldehydet er aldehydet som produseres industrielt i større mengder. Formaldehyd som oppnås ved oksydasjon av metanol anvendes i en 37% oppløsning av gass i vann under navnet formalin. Dette brukes i soling av skinn og i bevaring og balsamering av lik.
Formaldehyd også brukes som bakteriedreper, soppdreper og insektmiddel for planter og grønnsaker. Imidlertid er mest nyttig bidrag til fremstilling av polymermaterialet. Plastikken som kalles Bakelite, syntetiseres av reaksjonen mellom formaldehyd og fenol.
bakelitt
Bakelitt er en polymer av tredimensjonal struktur med stor hardhet som brukes i mange husholdningsredskaper som håndtakspotter, panner, kaffemaskiner, kniver mv.
Polymerer som ligner på bakelitt er laget av formaldehyd i kombinasjon med forbindelsene urea og melamin. Disse polymerene brukes ikke bare som plast, men brukes også som klebende lim og beleggmateriale.
kryssfiner
Kryssfiner er det kommersielle navnet på et materiale som er dannet av tynne treverk, kombinert med polymerer produsert av formaldehyd. Melmac Formica og merkevarer er laget med deltakelse av sistnevnte. Formica er et plastmateriale som brukes i møbelbelegg.
Melmac plast brukes til fremstilling av servise, briller, kopper, etc. Formaldehydet er råmateriale for syntese av forbindelsen metylen-difenyl-diisocyanat (MDI), forløper av polyuretan.
polyuretan
Polyuretan brukes som isolasjon i kjøleskap og frysere, polstring for møbler, madrasser, maling, lim, såler, etc.
butyraldehyd
Butyraldehydet er hovedforløperen for syntese av 2-etylheksanol, som brukes som en mykner. Den har en behagelig duft av eple tillate bruk i mat som smakstilsetning.
Også det brukes til produksjon av vulkaniseringsakseleratorer. Det involvert som et reaktivt mellomprodukt ved fremstilling av løsemidler.
acetaldehyd
Acetaldehyd ble benyttet i produksjonen av eddiksyre. Men denne rollen av acetaldehyd har gått ned i vekt fordi det har blitt fortrengt av metanolkarbonyliseringsprosessen prosessen.
syntese
Andre aldehyder er forløpere av oksoalkoholer, som brukes til fremstilling av vaskemidler. Såkalte oksoalkoholer fremstilles ved tilsetning av karbonmonoksyd og hydrogen til et olefin for å oppnå et aldehyd. Og til slutt aldehydet hydrogeneres for å oppnå alkoholen.
Noen aldehyder brukes til fremstilling av parfymer, som det er tilfelle av Chanel nr. 5. Mange aldehyder av naturlig opprinnelse har behagelige lukter, for eksempel: heptanal har en lukt av grønt gress; Octanal en oransje lukt; den nonanal en lukt av roser og citral en lukt av lime.
Eksempler på aldehyder
glutaraldehyd
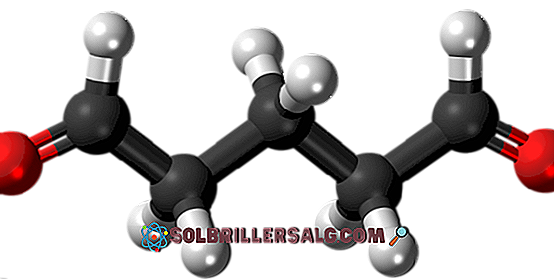
Glutaraldehyd har i sin struktur to formyls grupper i begge ender.
Markedsført under navnet Cidex eller Glutaral, brukt som et desinfeksjonsmiddel for sterilisering av kirurgiske instrumenter. Den brukes i behandling av vorter på foten, påført som en væske. Det er også brukt som et bindemiddel i vev histologiske og patologi laboratorier.
benzaldehyd
Det er den enkleste aromatiske aldehyd som er dannet av en benzenring i hvilken en formyl-gruppen er bundet.
Den finnes i mandelolje, derav karakteristisk lukt som gjør at du kan bruke som en mat smakstilsetning. I tillegg brukes den i syntese av organiske forbindelser relatert til fremstilling av legemidler og til fremstilling av plast.
glyseraldehyd
Det er et aldotriose et sukker består av tre karbonatomer. Den har to isomerer som kalles D- og L-enantiomerer. Glyceraldehydet er det første monosakkaridet som oppnås ved fotosyntese i den mørke fasen (Calvin-syklusen).
Glyseraldehyd-3-fosfat

Strukturen av glyceraldehyd-3-fosfat er illustrert i det øvre bildet. Røde kuler med gul tilsvarer fosfatgruppen, mens svart karbonskjelettet. Den røde kule knyttet til den hvite er OH-gruppen, men når den er knyttet til den svarte sfæren og den sistnevnte til den hvite sfæren, så er det CHO-gruppen.
Glyceraldehyd-3-fosfat involvert i glykolyse, en metabolsk prosess hvor glukose nedbrytes til pyruvinsyre med produksjon av ATP, et energibeholder av levende vesener. I tillegg er produksjonen av NADH, en biologisk reduksjonsmiddel.
I glykolyse stammer glyceraldehyd-3-fosfat og dihydroacetonfosfat fra spaltningen av D-fruktose-1-6-bisfosfat
Glyseraldehyd-3-fosfat er involvert i den metabolske prosess som er kjent som pentosen syklus. I denne NADPH er viktig biologisk redusering generert.
11-cis-retinal
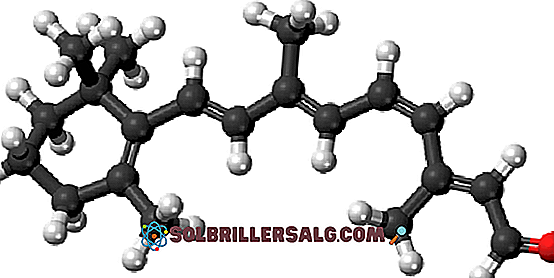
B-karoten er et naturlig pigment til stede i flere grønnsaker, spesielt i gulrøtter. Han gjennomgår en oksidativ brudd i leveren, som omdannes til alkoholretinol eller vitamin A. Oksidasjonen av vitamin A og den etterfølgende isomerisering av en av sine dobbeltbindinger danner 11-cis-retinalaldehydet.
Pyridoxalfosfat (vitamin B6)
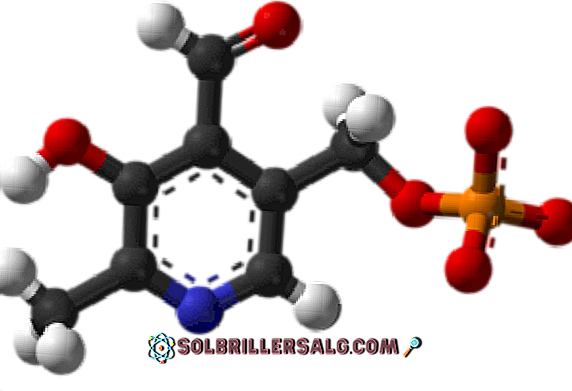
Det er en protetisk gruppe knyttet til flere enzymer, som er den aktive formen av vitamin B6 og deltar i synteseprosessen av den inhibitoriske nevrotransmitteren GABA.
Hvor er formylgruppen i sin struktur? Legg merke til at dette er forskjellig fra resten av gruppene knyttet til den aromatiske ringen.
salicylaldehyd
Det er et antipyretisk råmateriale for syntese av acetylsalisylsyre, og smertestillende stoff som er kjent som Aspirin.







